 |
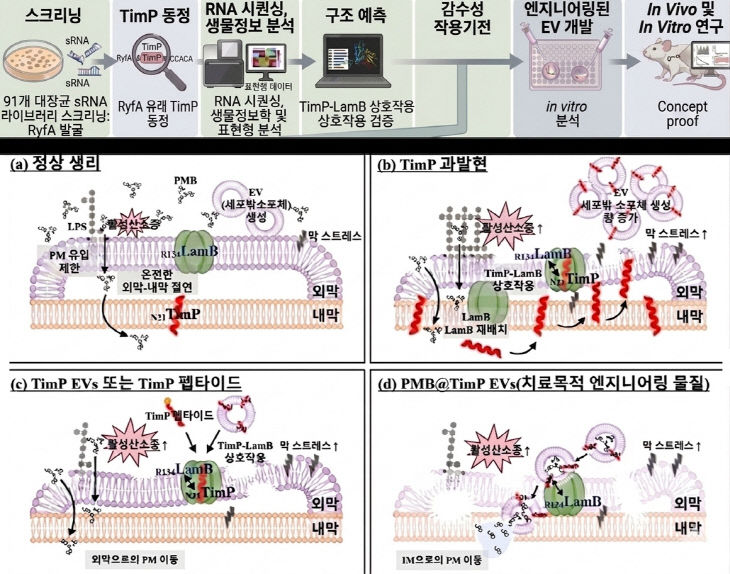
| 부산대학교 김광선 교수 연구팀이 제시한 다제내성 그램음성균 제어 전략 모식도.(사진=부산대 제공) |
더 강한 항생제를 찾는 대신, 세균 자체의 구조를 흔들어 약물이 스며들도록 만드는 접근이다.
부산대학교 연구진은 다제내성 그램음성균을 대상으로, 세균이 가진 외막 방어 체계를 스스로 약화시키는 방식의 치료 전략을 제시했다.
이 방법은 항생제 자체를 바꾸지 않으면서도 효과를 끌어올릴 수 있다는 점에서 새로운 가능성을 보여준다.
◆ '공격' 아닌 '유도'…치료 패러다임 전환
연구팀은 대장균의 유전자 조절 과정에서 유래한 펩타이드 'TimP'에 주목했다.
이 물질은 세균 외막 구조를 변화시키는 역할을 하며, 결과적으로 항생제가 내부로 들어갈 수 있는 환경을 만든다.
특히 TimP가 많이 생성되는 상황에서는 세균이 세포밖 소포체(EV)를 다량으로 만들어내는데, 이 구조가 외막을 재구성하는 데 관여하는 것으로 나타났다.
일종의 '자기 붕괴 유도 장치'가 작동하는 셈이다.
이 과정에서 항생제 폴리믹신은 기존보다 훨씬 쉽게 세균 내부로 침투할 수 있게 된다.
그동안 외막 장벽 때문에 효과가 제한적이었던 약물이 새로운 통로를 확보하게 되는 구조다.
◆ 기존 약물 재활용…효율·안전성 동시에 확보
연구진은 이러한 메커니즘을 실제 치료 전략으로 확장해, TimP와 폴리믹신을 함께 담은 전달체를 구축했다.
해당 플랫폼은 낮은 농도의 항생제로도 높은 항균 효과를 보였으며, 독성 문제 역시 줄일 수 있는 가능성을 확인했다.
기존에는 여러 항생제를 조합하는 방식이 주로 시도됐지만, 약물 간 상호작용이나 체내 분포 차이로 실제 적용에 어려움이 많았다.
반면 이번 접근은 세균 구조 자체를 바꾸는 데 초점을 맞춰 이러한 한계를 우회했다는 평가다.
연구팀은 세균 외막 단백질과 TimP 간 상호작용을 분석해, 외막이 물리적으로 재배열되는 과정을 규명했다.
이러한 반응이 특정 균주에 국한되지 않고 공통적으로 나타날 수 있다는 점도 함께 제시됐다.
이번 연구는 항생제 개발의 방향을 '신약 탐색'에서 '기존 자원의 재설계'로 확장했다는 데 의미가 있다.
연구를 이끈 김광선 교수는 "세균의 방어 체계를 정밀하게 조절해 약물 투과성을 높인 점이 핵심"이라며 "항생제 사용량을 줄이면서 치료 효과를 높일 수 있는 전략"이라고 설명했다.
한편 이번 성과는 한국연구재단 지원과 한국생명공학연구원과의 협력을 통해 진행됐으며, 관련 연구 결과는 약물 내성 분야 국제 학술지에 게재됐다.
부산=김성욱 기자
중도일보(www.joongdo.co.kr), 무단전재 및 수집, 재배포 금지
 김성욱 기자
김성욱 기자










![[영상]빙그레 장종훈 유니폼부터 류현진 한정판, 꿈돌이 문현빈까지 당신의 유니폼에 담긴 사연은?](https://dn.joongdo.co.kr/mnt/images/webdata/content/2026y/04m/28d/20260426001006025_1.jpg)





